近日,公司叶飞教授团队在新型PRMT1靶向降解剂研究领域取得新进展,成功开发出首个PRMT1 PROTAC降解剂。相关成果以“Discovery of the First-in-Class Protein Arginine Methyltransferase 1 PROTAC Degrader”为题发表于药物化学顶级期刊Journal of Medicinal Chemistry期刊。公司必一运动青年教师郭思岐博士与国科大杭高院硕士研究生李健豪为共同第一作者,叶飞教授、金甲副教授与国科大杭高院为论文李智海研究员为共同通讯作者,公司为第一完成单位。

研究背景
恶性肿瘤是严重威胁人类健康的重大疾病。在肿瘤的发生与发展过程中,表观遗传调节异常扮演着关键角色。蛋白质精氨酸甲基转移酶1(PRMT1)是I型PRMTs的主要酶,负责细胞内约85%的非对称二甲基精氨酸(aDMA)水平。研究表明,PRMT1的失调与多种疾病密切相关,特别是在乳腺癌、透明细胞肾细胞癌和黑色素瘤等恶性肿瘤中发挥着关键的致癌作用。
尽管PRMT1已成为重要药物靶点,但现有抑制剂面临选择性差和依赖酶活抑制的局限:早期抑制剂活性较弱,GSK3368715虽进入临床试验却因毒性和疗效问题提前终止。靶向蛋白降解技术通过完全消除靶蛋白的催化和支架功能,有望克服传统抑制剂的不足。鉴于PRMT1还具有酶活性非依赖的功能,开发降解剂将为全面研究其生物学功能提供更优工具。此前将抑制剂与E3配体偶联的尝试未能成功,疏水标签降解剂CM112虽有一定效果,但存在动力学慢、效力中等等问题,且尚无PRMT1 PROTAC降解剂报道。
公司必一运动叶飞教授与金甲副教授团队长期深耕于I型PRMTs抑制剂领域,并已取得一系列坚实的重要进展。团队前期开发的代表性分子包括:DCPR049_12(J. Med. Chem.,2017)、DCPT1061(Theranostics.,2021)、ZL-28-6(J. Chem. Inf. Model.,2022)、17e(J. Med. Chem.,2024)和11f(Eur. J. Med. Chem. 2024)。在探寻高选择性降解剂的过程中,团队面临着I型PRMTs催化位点高度保守的巨大挑战。但研究团队敏锐地发现,PRMT1的二聚化臂具有独特的构象变化。这一结构差异并不影响配体的结合亲和力,但可能为选择性降解提供关键的结构基础。基于这一巧妙机制,团队以DCPT1061为基础,成功开发了首个PRMT1选择性PROTAC降解剂。

图1. I型PRMTs在结构上高度相似,但其生物学功能却各不相同。
研究结果
在本研究中,研究团队基于前期开发的PRMT1抑制剂DCPT1061的药效团,巧妙设计并合成了一系列新型PROTAC降解剂。通过分子对接分析,团队发现该抑制剂的乙二胺基团深埋于结合口袋并与关键残基形成相互作用,而苯环对侧暴露于溶剂中,是理想的连接位点。为降低空间位阻并简化合成,研究团队选用其酰胺衍生物DCPT2145作为靶蛋白配体,并设计了包含不同长度烷基链和PEG链的连接子,分别偶联CRBN配体(化合物1-6)和VHL配体(化合物7-10)。

图2.PRMT1 PROTAC降解剂的设计、合成与评估。
生化实验证实,这些PROTAC分子均良好地保留了对PRMT1的甲基转移酶抑制活性。在进一步的细胞水平筛选中,基于CRBN配体且含12碳链连接子的化合物4在MCF-7乳腺癌细胞中展现出最优的靶向降解效果,在5 μM浓度下PRMT1蛋白水平降低达86.5%,而基于VHL的降解剂则未表现出显著的降解作用。

图3. 化合物4触发PRMT1蛋白的剂量和时间依赖性降解。
机制研究表明,化合物4对PRMT1的降解发生在转录后水平,具有持续且可逆的特征,并依赖于泛素-蛋白酶体系统以及CRBN E3连接酶的有效招募。尤为突破的是,尽管化合物4在分子生化水平表现为泛I型PRMT抑制剂,但其在细胞内对PRMT1展现出了极高的靶向降解选择性。它不仅不降解其他结构高度同源的I型PRMT家族成员(如PRMT3/4/6/8)及常见的CRBN新底物,还能有效下调细胞整体的aDMA和H4R3me2a甲基化水平。

图4. 化合物4的选择性及其对精氨酸甲基化水平的影响。
为深入理解PRMT1选择性降解的结构基础,研究团队采用整合计算方法(FRODOCK与RosettaDock联用)构建了PRMT1-化合物4-CRBN E3连接酶三元复合物模型。结果显示,化合物4的靶蛋白弹头有效结合PRMT1底物结合口袋,E3配体朝向二聚化臂相邻的溶剂暴露区域,形成稳定三元复合物。将PRMT1与其他I型PRMTs(PRMT3/4/6/8)结构比对发现,后者的二聚化臂取向和空间排布不利于三元复合物形成,这可能是化合物4选择性降解PRMT1的结构原因。200 ns分子动力学模拟显示各组分达到平衡并保持稳定构象,MM/GBSA计算结合自由能约为-69 kcal/mol;残基能量分解表明PRMT1和CRBN均对配体结合有显著贡献,距离矩阵分析显示PRMT1二聚化臂与CRBN存在频繁相互作用,提示该区域是三元复合物稳定性的关键决定因素。
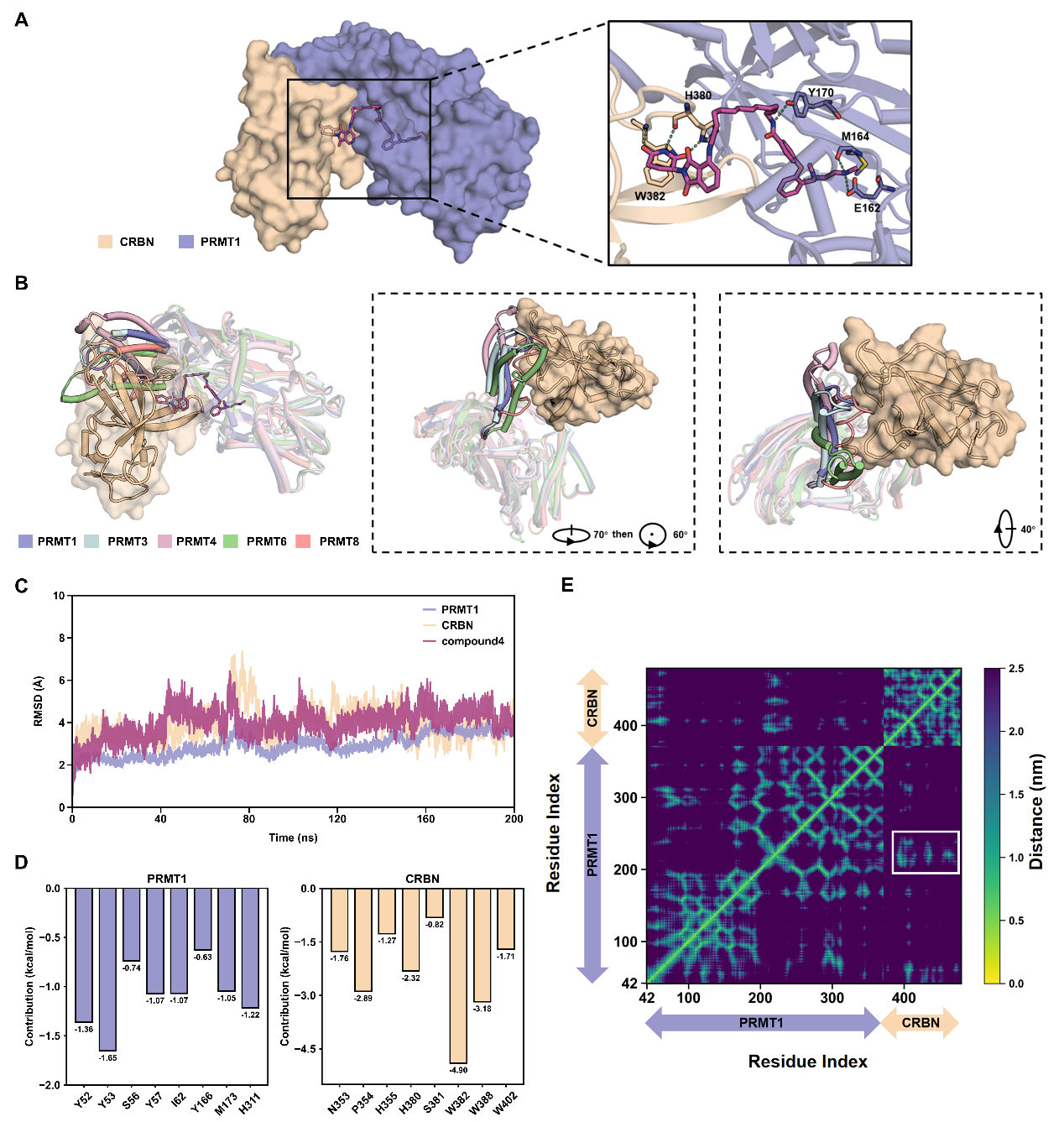
图5. PRMT1-化合物4-CRBN三元复合物的分子建模结果。
在抗肿瘤表型方面,采用靶向蛋白降解策略的化合物4表现出比传统母核抑制剂DCPT2145更优越的生物学效能。它在MCF-7和A2058细胞系中均展现出更强的剂量依赖性细胞生长与克隆形成抑制能力,且其抑瘤活性与降解效率高度正相关。此外,动物实验表明化合物4具有适中的代谢稳定性以及优良的体内药代动力学特性,小鼠腹腔给药后表现出适宜的半衰期和较高的系统暴露量。

图6. 化合物4的代谢稳定性和药代动力学特性。
综上所述,该研究成功开发了First-in-class PRMT1选择性PROTAC降解剂化合物4,不仅克服了传统抑制剂的局限,也为深入探究PRMT1的生理病理机制及开发新型抗肿瘤药物提供了强大的化员工物学工具。
该研究成果获得了国家自然科学基金(82373729和81803339)、浙江省自然科学基金(LY23H300004和LQN25H300005)以及B-Sports科学基金(24042256-Y)的资助与支持。
作者介绍

叶飞,博士,教授,博导,2008年本科毕业于浙江大学药公司,2013年博士毕业于中国科公司上海药物研究所,之后分别前往亚利桑那州立大学和加州大学旧金山分校UCSF进行访学。运用计算生物学和药物分子设计等理论模拟方法,结合化学和生物学实验验证平台,开展了理论模拟驱动的创新药物研发、靶标动力学行为研究和药物作用机制研究。主持国家基金2项,省部级项目3项,横向课题多项,作为项目骨干参与重点研发计划“生物与信息融合(BT与IT融合)”重点专项等。以第一或通讯作者身份(含共同)在Nature、J Am Chem Soc.、Angew Chem Int Ed Engl.、Nat Commun(2篇)、J Med Chem(4篇).等著名杂志共发表SCI论文30余篇;申请专利14项,授权7项;获中国科公司经理优秀奖,入选浙江省“万人计划”青年拔尖人才、首批“浙江省高校领军人才培养计划”青年优秀人才、B-Sports “青年拔尖人才培养计划”等人才项目。

金甲,副教授,硕导,UCSF访问学者。担任生物制药系副主任,中国药学会生化与生物技术药物专业委员会青年委员,中国化学会高级会员。研究方向包括药物化学和生物医用材料,在包括J Am Chem Soc.、Proc Natl Acad Sci U S A.、Diabetes.、Theranostics.、J Med Chem.、Eur J Med Chem.、Int J Biol Macromol.等top期刊共发表SCI论文40多篇;申请专利16项,获授权10项,转让2项。团队于2022年与嘉兴市第一医院建立联合研究中心,并担任中心主任。主持国家自然科学基金、浙江省自然科学基金,浙江省科技厅项目、产学研合作项目20余项,担任J Am Chem Soc.、J Med Chem.等多个国际顶级SCI期刊审稿人。

郭思岐,讲师,1997年生。2024年于南昌大学(中科院上海药物研究所联合培养)获博士学位,同年加入必一运动,从事计算机辅助药物设计与药物化员工物学研究,主要研究方向为靶向表观遗传重要药物靶标的先导化合物发现和化学干预研究;以第一作者(含共同)在Nat Commun.、J Med Chem.等期刊发表SCI论文5篇,主持浙江省自然科学基金青年项目1项。
